کربن فعال چیست؟
کربن فعال یا زغال فعال عنصر متخلخلی است که ترکیبات عمدتاً آلی موجود در گاز یا مایع را به دام می اندازد. این کار را با چنان اثربخشی انجام می دهد که پرکاربردترین عامل تصفیه کننده توسط انسان است.
ترکیبات آلی از متابولیسم موجودات زنده به دست می آیند و ساختار اصلی آنها از زنجیره ای از اتم های کربن و هیدروژن متشکل است. از جمله تمام مشتقات دنیای نباتی و جانوری از جمله روغن و ترکیبات حاصل از آن است.
خاصیت یک جامد برای چسبیدن یک مولکول در حال جریان به دیواره های خود را "جذب" می گویند. جامد را "جاذب" و مولکول "جذب" نامیده می شود.
پس از فیلتراسیون که برای حذف جامدات موجود در یک سیال در نظر گرفته شده است - هیچ فرآیند خالص سازی با کاربردهای بیشتر از کربن فعال وجود ندارد.
کاربرد کربن فعال چیست؟
تصفیه آب
کربن فعال آفتکشها، چربیها، روغنها، مواد شوینده، محصولات جانبی ضدعفونی، سموم، ترکیبات تولیدکننده رنگ، ترکیبات تولید شده از تجزیه جلبکها، سبزیجات یا متابولیسم حیوانات را حفظ میکند.
بو زدایی و تصفیه هوا
به عنوان مثال در ماسکهای کارتریجی، سیستمهای گردش هوا در فضاهای عمومی، دریچههای زهکشی و تصفیهخانههای آب، غرفههای کاربرد رنگ، فضای ذخیرهسازی کلاه یا استفاده از حلالهای آلی.
درمان افراد مبتلا به مسمومیت حاد
کربن فعال یک "پادزهر جهانی" در نظر گرفته می شود و در اورژانس ها و بیمارستان ها استفاده می شود.
تصفیه شکر
زغال سنگ پروتئین هایی را حفظ می کند که به آب نیشکر رنگ می دهند. هدف اصلی این فرآیند جلوگیری از تخمیر و فاسد شدن شکر است.
حذف رنگ روغن گیاهی
رنگ را از روغن نارگیل، گلوکز ذرت و سایر مایعات مورد استفاده در صنایع غذایی پاک می کند.
رفع بو و حذف رنگ تقطیر الکلی
رنگ و بو را از شراب های انگور پاک می کند و عرقیات از منابع دیگر را از بین می برد.
بازیابی طلا
طلایی که با فرآیند شناورسازی از مواد معدنی جدا نمی شود، در سیانید سدیم حل شده و به کربن فعال جذب می شود.
کربن فعال چگونه کار می کند و چه فوایدی دارد؟
کربن فعال یک محیط جاذب است، وظیفه آن جذب مولکول های آلی در ریز منافذ آن است. با استفاده از فرآیندهای حرارتی یا شیمیایی برای افزایش ظرفیت جذب آن فعال می شود.
توضیح گرافیکی ساده در مورد نحوه عملکرد کربن فعال را در زیر مشاهده می کنید.
از سوی دیگر، کربن فعال جاذب نیست را در تصاویر زیر مشاهده می کنید.
چه چیزی به کربن فعال خاصیت جذب، عمدتاً مولکول های آلی می دهد؟
هر ذره کربنی قابلیت جذب دارد. به همین دلیل است که برخی افراد برای از بین بردن بوها، کربن را در یخچال قرار می دهند. اگر کربن را در یک ظرف آب قرار دهید، همین امر صادق است: رنگ، طعم و بو را از بین می برد. یا در حومه شهر، مردم تورتیلا را می سوزانند و برای رفع مشکلات گوارشی (مانند عفونت های خفیف، سوء هاضمه یا نفخ آن) می خورند.
فعال کردن کربن شامل متخلخل ساختن آن برای افزایش ظرفیت جذب آن است. یک گرم کربن دارای مساحتی در حدود 50 متر مربع است. با فرآیند فعال سازی به 600 یا 800 متر مربع می رسد. یعنی بین 12 تا 16 برابر افزایش می یابد.
اتم های کربن
اتمهای کربنی که جامدی را تشکیل میدهند که ما آن را «کربن» مینامیم، توسط پیوندهای کووالانسی به یکدیگر متصل میشوند. هر اتم یک الکترون با چهار اتم کربن دیگر به اشتراک می گذارد (به یاد داشته باشید که در کران های یونی، الکترونگاتیوترین اتم یک یا چند الکترون را از دیگری می دزدد).
اتم هایی که روی سطح نیستند، چهار پیوند خود را در همه جهات توزیع می کنند. اما اتم های سطحی، اگرچه به چهار اتم دیگر متصل هستند، اما در فضای کمتری مجبور به انجام این کار می شوند و عدم تعادل نیروها در آنها باقی می ماند. این عدم تعادل همان چیزی است که آنها را با ،به دام انداختن مولکولی از مایعی که کربن را احاطه کرده است، سوق می دهد.
نیروی لندن
نیرویی که اتم کربن سطح دیگری را به دام می اندازد، "نیروی لندن" نامیده می شود که یکی از هفت نوع "نیروهای وان در والس" است. این یک پیوند فیزیکوشیمیایی در نظر گرفته میشود، به اندازهای قوی که بتواند جذبکننده را حفظ کند، اما نه آنقدر قوی که به عنوان یک پیوند شیمیایی برگشتناپذیر در نظر گرفته شود که ساختار مولکولی جدیدی را تشکیل میدهد. بنابراین، جذب برگشت پذیر است و کربن فعال می تواند دوباره برای استفاده فعال شود.
همانطور که گفتیم، مولکول هایی که کربن جذب می کند تمایل به پیوند کووالانسی دارند و پیوند آتها یونی نیست، زیرا دومی سعی می کند الکترون ها را بدزدد یا به اتم های کربن اهدا کند. پیوندهای بین اتم های کربن و هیدروژن کووالانسی هستند و به همین دلیل است که کربن جاذب خوبی برای مولکول های آلی است.
همه مولکول های آلی تمایل به کووالانسی ندارند. آنها معمولاً حاوی اکسیژن، گوگرد و سایر اتمهای الکترونگاتیوی بالا هستند که به بخشی از مولکول که آنها را در بر می گیرد تمایل یونی می دهد. از سوی دیگر، همه مولکول های معدنی تمایل به یونی ندارند و تمایل کووالانسی دارند. در مورد دی سیانید طلا که کربن فعال را به بخشی ضروری از فرآیند استخراج این فلز گرانبها تبدیل می کند، چنین است.
از کدام مواد خام می توان کربن فعال به دست آورد؟
در تئوری، هر ذره کربنی می تواند فعال شود. با این حال، اگر کربن بسیار منظم باشد (مانند الماس یا گرافیت)، حذف برخی اتمهای کربن برای ایجاد منافذ دشوار است.
یکی از راههای طبقهبندی کربنها بر اساس ترتیب اتمهای کربن آنها است. هرچه سفارش کمتری داشته باشد، سختی کربن کمتر است و به راحتی می توان آن را فعال کرد.
پوسته نارگیل و زغال چوب
متداولترین مواد خام مورد استفاده برای تولید کربن فعال عبارتند از: چوبهای نرم (مانند کاج)، کربنهای معدنی زغال سنگ (زغالسنگ، قیر و آنتراسیت) و پوستهها یا استخوانهای گیاهی (پوسته نارگیل، چالههای زیتون یا هلو، پوست گردو).
کربنهای فعال ساخته شده از چوبهای نرم، منافذ با قطر بزرگ را تشکیل میدهند و برای رنگدهی مایعات مناسب هستند.
زغال سنگ معدنی
آنهایی که از زغال سنگ ساخته می شوند، تمایل دارند طیف وسیعی از منافذ را تشکیل دهند. آنها معمولاً برای کاربردهایی که ترکیباتی که باید حفظ شوند دارای اندازه های مولکولی مختلف هستند مناسب تر هستند.
آنهایی که از پوسته یا استخوان سخت به وجود می آیند، منافذ کوچکی را تشکیل می دهند و در تصفیه گازها یا در تصفیه آب خروجی از چاه ها به کار می روند.
شکل فیزیکی کربن فعال چیست؟

کربن را می توان به صورت پودر، گرانول یا گلوله های استوانه ای تولید کرد.
کربن پودری فقط در تصفیه مایعات استفاده می شود. زغال سنگ در یک مخزن با هم زدن ریز می شود و سپس با استفاده از یک فیلتر مناسب برای حفظ ذرات کوچک (مانند فیلتر پرس) از مایع جدا می شود.
در مورد زغال سنگ دانه ای در محدوده های ذرات مختلفی تولید می شود که بر اساس اندازه ذرات یا عدد مش مشخص می شود. به عنوان مثال، مش 4، مشکی است که در هر اینچ خطی چهار سوراخ دارد. آنها هم در تصفیه مایعات و هم در گازها کاربرد دارند.
گلوله ها معمولاً در تصفیه گاز استفاده می شوند، زیرا شکل استوانه ای آنها افت فشار کمتری ایجاد می کند.
اگر کربن یا گلوله دانه ای مورد نظر باشد وماده خام به اندازه کافی سخت نباشد، می توان آن را با استفاده یک ماده اتصال دهنده که به آن قوام می دهد تقویت کرد تا از شکستن آن هنگام عبور سیال جلوگیری کند.
کربن چگونه فعال می شود؟
فرایند حرارتی
کربن را می توان با فرآیندهای حرارتی یا شیمیایی فعال کرد. فرآیندهای حرارتی شامل تحریک اکسیداسیون جزئی کربن، برای رسیدن به تشکیل منافذ، اما اجتناب از ایجاد گاز و از دست دادن کربن بیشتر از حد لازم است. این در دماهای بین 600 تا 1100 درجه سانتیگراد (1112 درجه فارنهایت و 2012 درجه فارنهایت) و در اتمسفر کنترلی (که با تزریق مقدار مناسبی از بخار آب یا نیتروژن حاصل می شود) رخ می دهد.
فرایند شیمیایی
قبل از کربن شدن فرآیندهای شیمیایی از مواد خام شروع می شود. این معرف ها عوامل کم آب کننده (مانند اسید فسفریک) هستند که پیوندهایی را که زنجیره های سلولزی را به یکدیگر متصل می کنند، می شکنند. پس از این مرحله، مواد در دمای نسبتاً پایین (حدود 550 درجه سانتیگراد یا 1022 درجه فارنهایت) کربنیزه و سپس برای حذف بقایای معرف و سایر محصولات جانبی شسته هستند.
کوره هایی که در آنها کربن به صورت حرارتی فعال است یا کربنی که قبلاً با یک ماده شیمیایی کربنیزه است، می توانند دوار یا عمودی (مرحله ای) باشند.
ظرفیت جذب کربن فعال چقدر است؟
ظرفیت یک کربن فعال برای حفظ یک ماده معین نه تنها با مساحت سطح آن مشخص میشود، بلکه با نسبت منافذی که اندازه مناسبی دارند نیز مشخص میشود، یعنی یک کربن مناسب قطری بین یک تا پنج برابر مولکول مورد نظر دارد.
زغال فعال در دکلره چگونه عمل می کند؟
دکلره یک مکانیسم پیچیده دارد و مسیرهای واکنش مختلفی را دنبال می کند که در آن کربن فعال می تواند به عنوان یک واکنش دهنده یا یک کاتالیزور دخالت کند.
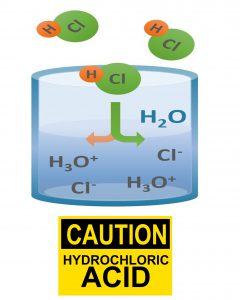
کلر آزاد را می توان به صورت گاز کلر، محلول هیپوکلریت سدیم یا جداول هیپوکلریت کلسیم (گرانول) به آب اضافه کرد.
در هر یک از این موارد، کلر به شکل اسید هیپوکلرو (HOCl) حل می شود، اسید ضعیفی که تمایل به تجزیه جزئی دارد.
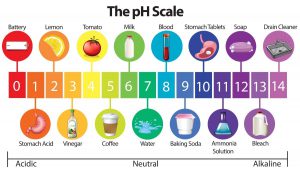
توزیع بین اسید هیپوکلروس و یون هیپوکلریت به pH و غلظت این گونه ها بستگی دارد. هر دو شکل مولکولی به عنوان کلر آزاد تعریف می شوند.
هر دو اکسیدان قوی هستند که وقتی به آب اضافه میشوند تقریباً بلافاصله با ناخالصیهای آلی و معدنی واکنش نشان میدهند و یک اثر بیوسیدال روی میکروارگانیسمها اعمال میکنند.
کلری که واکنش نشان می دهد و آن که در این مرحله از گندزدایی مداخله می کند، آزاد نمی ماند و ترکیب می ماند و آزاد نمی ماند. هنگامی که این مرحله به پایان رسید، لازم است کلر آزاد باقیمانده را با استفاده از کربن فعال دانه ای حذف کنید.
هنگامی که کربن در معرض کلر آزاد قرار می گیرد، واکنش هایی رخ می دهد که در آن HOCl یا OCl به یون کلرید کاهش می یابد. این کاهش نتیجه مسیرهای مختلف واکنش های ممکن است.
در دو مورد از رایج ترین آنها، GAC بر اساس واکنش های زیر عمل می کند:
جایی که C نشان دهنده کربن فعال است. CO و CO2 اکسیدهای سطحی هستند که به تدریج فضاهایی را اشغال می کنند که در صورت مسدود شدن، دیگر در واکنش شرکت نمی کنند. برخی از این اکسیدها به صورت CO و CO2 در محلول آزاد می شوند. این کار دوباره فضاهایی را در دسترس می گذارد که بنابراین ظرفیت کربن فعال دانه ای برای این واکنش را افزایش می دهد.
در مورد کلر نیز در اولین لحظات عملیات روی سطح زغال سنگ تجمع می یابد. با ادامه رسیدن HOCl یا OCl به سطح کربن، سرعت واکنش کمی کاهش می یابد و سپس کلر شروع به آزادی می کند. این کاهش سرعت به دلیل مسمومیت کربن توسط اکسیدهای سطحی است. این مسمومیت به تدریج ادامه می یابد، در حالی که ظرفیت جذب و کلر زدایی کربن فعال کاهش می یابد.
در واکنش های فوق می توانید به جای HOCl مداخله کنید، با این تفاوت که H+ تولید نمی شود. مشاهده می شود که کربن فعال واکنش نشان می دهد و بنابراین ناپدید می شود. اگر اکسیدهای سطحی انباشته نمی شد، واکنش تا ناپدید شدن کامل کربن ادامه می یافت.
چه نوع کربنی برای سفید کردن مناسب است؟
رنگ هایی که در مایعات ظاهر می شوند معمولاً مولکول های نسبتاً بزرگی هستند. بنابراین، آنها در منافذ بزرگ جذب می شوند، که باعث می شود کربن برای حفظ آنهایی که دارای بیشترین تخلخل هستند، مناسب تر باشد.
زغال چوب، به ویژه آنهایی که از چوب های نه چندان سخت (مانند کاج) که از نظر شیمیایی فعال می شوند، بیشترین درشت تخلخل را دارند و بنابراین مناسب ترین برای تغییر رنگ هستند.
مشکل این کربن ها این است که خیلی سخت نیستند و در برابر سایش مقاومت چندانی ندارند، به این معنی که باید به صورت پودر اعمال شوند. هنگامی که کربن سفید کننده نیاز به دانه بندی دارد، بهترین جایگزین معمولاً کربن لیگنیت است. این کربن با بیشترین درشت تخلخل است.
کدام نوع کربن فعال برای تصفیه آب مناسب است؟
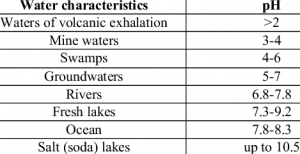
آلاینده هایی که معمولاً در آب چاه وجود دارند معمولاً با وزن مولکولی کم هستند و برای این موارد مناسب ترین کربن کربنی با ریزتخلخل بالا است.
کربن هایی که به بهترین وجه این شرایط را برآورده می کنند، اولاً کربن های پوسته نارگیل و متعاقباً مواد معدنی قیر هستند.
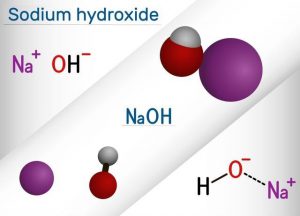
چرا هنگام نصب کربن بکر، pH آب تغییر می کند؟
هنگامی که یک کربن با مواد شیمیایی فعال است، حذف تمام مواد شیمیایی مورد استفاده از محصول نهایی برای سازنده غیرعملی و غیر ضروری است. بنابراین، اگر ماده شیمیایی یک اسید باشد، pH اولین لیتر آبی را که با کربن تماس پیدا می کند، کاهش می دهد. اگر ماده شیمیایی مورد استفاده قلیایی باشد برعکس اتفاق می افتد.
در مورد کربن فعال حرارتی (بدون وجود مواد شیمیایی غیر از بخار آب و گازهای حاصل از احتراق)، pH اولین لیتر آب تصفیه با آن افزایش می یابد.
زیرا همه سبزیجات دارای مقادیر قابل توجهی سدیم، پتاسیم، کلسیم و سایر کاتیون ها هستند که در فرآیند کربنیزاسیون، به شکل اکسید در کربن باقی می مانند. این اکسیدها در تماس با آب به هیدروکسید تبدیل می شوند و در آب حل می شوند و PH آن را افزایش می دهند.
هنگامی که PH اولین لیتر آبی که با کربن تماس پیدا می کند تغییر نمی کند، می تواند یک کربن با pH تنظیمی یا یک کربن فوق خالص (بدون محلول) باشد.
تماس با ما: